По данным информационного бюллетеня ВОЗ, ежегодно рождается 5% детей с наследственными заболеваниями и врожденными патологиями, из них которых хромосомными мутациями обусловлено до 1%.
Что такое и почему возникают хромосомные болезни
Человеческий организм состоит из миллионов клеток, каждая из которых имеет ядро с нуклеопротеидными структурами − хромосомами, состоящими из длинных двухцепочечных молекул ДНК. На них располагается множество генов, которые несут «инструкции» для нормального роста, развития и функционирования организма, а также отвечают за большое количество признаков (цвет волос, глаз и др.).
При слиянии половых клеток, 23 хромосомы передаются будущему ребенку от матери и 23 − от отца, поэтому в нормальном кариотипе (хромосомном наборе) человека 46 хромосом. Они составляют пары: 22 пары неполовых (аутосом) и 23-я пара половая (XX − у женщин и XY − у мужчин). Хромосомный «сбой» может произойти случайно в процессе мейотического деления половых клеток одного из родителей (яйцеклетке и сперматозоиде) еще до зачатия или на раннем этапе развития оплодотворённого яйца.
В большинстве случаев хромосомные болезни возникают в результате изменения количества и структуры хромосом. Хотя причиной также может стать носительство родителей сбалансированных перестроек в хромосомах без изменения кариотипа. В этом случае человек внешне абсолютно здоров, а проблемы выявляются только при желании зачать ребенка и проявляются бесплодием, неудачными попытками ЭКО, невынашиванием беременности, мертворождением или рождением ребенка с патологиями.
В 90% случаев хромосомные нарушения выявляются в детском и подростковом возрасте. Но некоторые из них диагностируются только после наступления половой зрелости.
Количественные хромосомные аномалии
Такие нарушения возникают, когда в наборе происходит мутация, которая приводит к увеличению или, напротив, уменьшению числа копий хромосом. Нарушения могут произойти в любой из пар хромосом (аутосомных или половых). Наличие одной лишней хромосомы называется «трисомия», более − «полисомия» (2-х − «тетрасомия», 3-х − «пентасомия» и т. д.), а отсутствие − «моносомия».
Среди наиболее распространённых заболеваний, вызванных изменением числа хромосом, синдром Дауна (трисомия 21), Эдвардса (трисомия 18) и Патау (трисомия 13). Такие болезни проявляются задержкой физического и умственного развития, пороками внутренних органов и различными уродствами.
Отсутствие одной половой хромосомы у женщин проявляется синдромом Шерешевского-Тёрнера, а дополнительная одна или более женских хромосом у мужчин становится причиной синдрома Клайнфельтера. При таких хромосомных болезнях возникает задержка полового развития и бесплодие.
Патологии также проявляются дополнительным гаплоидным хромосомным набором (полиплодии), то есть когда половая клетка содержит полный диплоидный набор из 46 хромосом, вместо 23. Такие хромосомные мутации почти всегда приводят к внутриутробной гибели плода.
Хромосомные заболевания могут проявляться в мозаичной форме. В этом случае дополнительная хромосома присутствует только в части клеток человека. При мозаицизме обычно болезнь протекает в легкой форме, а симптоматика зависит от % клеток с дублированием.
Структурные хромосомные нарушения
Такие «ошибки» обусловлены внутри- и межхромосомными перестройками (аберрациями). В фазе клеточного деления хромосома визуально напоминает букву «Х». Она имеет сложное строение из двух хроматид и первичной перетяжки (центромеры), за счет которой образуются короткие и длинные плечи.
В результате «сбоев» могут произойти различные изменения в структуре хромосом, среди которых наиболее распространены следующие нарушения.
- Дупликации − дополнительная копия (удвоение) части хромосомы, что приводит к избытку генетической информации.
- Транслокации − фрагмент хромосомы перенесен на другую. Если она копируется частично, симптоматика болезни обычно выражена менее серьёзно, чем при полной трисомии.
- Инверсии − поворот участка на 180°, в результате чего гены в этом фрагменте располагаются в обратном порядке. Может локализоваться по одну или по разные стороны от центромеры.
- Инсерции − вставка фрагмента «на не свое место».
- Делеции − фрагмент концевого или внутреннего участка хромосомы утрачен или укорочен и, следовательно, потеряна часть генетической информации. Нарушение может быть любого размера (микро и макро), а также произойти в любом локусе.

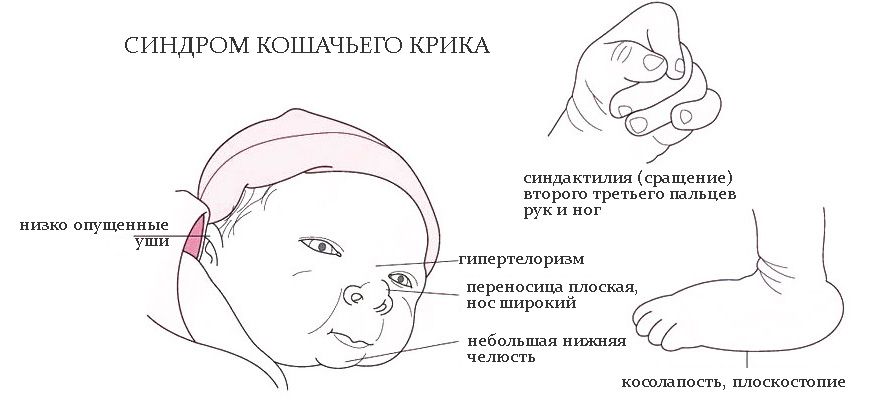
Делеции становятся причиной синдромов Лежёна (кошачьего крика), Вольфа-Хиршхорна, Прадера-Вилли, Смита-Магениса. Но не всегда аберрации проявляются проблемами со здоровьем. Ребенок может унаследовать сбалансированную перестройку, которая, как и у его родителя, не повлияет на качество жизни.
Из хромосомных патологий, которые становятся причиной гибели плода, на долю полных аутосомных трисомий приходится около 60%. До 20% заболеваний вызваны полиплодиями и до 15% − моносомией X хромосомы. Реже к самопроизвольным абортам приводят структурные перестройки, в частности транслокации и делеции.
Факторы риска
В последние десятилетие изучению этиологии хромосомных болезней уделяется большое внимание. По наследству патология передается только в 3-5% случаях, а большинство мутаций происходит в хромосомах спонтанно на этапе формирования половых клеток или после оплодотворения (de novo). Каковы их причины пока неизвестно, но среди усугубляющих факторов геномных мутаций ионизирующее излучение, химические мутагены (химвещества, лекарственные препараты с мутагенным эффектом), вирусные инфекции (краснуха, ветряная оспа, вирусный гепатит и др.).
Риск рождения больного ребенка также увеличивают такие биологические факторы, как:
- Возраст женщины − после 35 лет резко возрастает вероятность мутаций. Вероятно, это связано с тем, что с возрастом в женском организме истощается запас яйцеклеток, которые пригодны для оплодотворения, а в их ДНК накапливаются различные «повреждения». Если частота вероятности синдрома Дауна у женщин в возрасте 25 лет равен 1:1300, то в 45 лет этот показатель составляет 1:30.
- Отягощенный семейный анамнез − в семье уже есть больной ребенок, то риск развития заболевания у плода увеличивается на 1%.
- Невынашивание беременности − риск повышается в случае нескольких предшествующих выкидышей или мертворождения из-за врожденных дефектов развития, так как около 30% из них имеют аномалии в хромосомах.
Диагностика
По приказу Министерства здравоохранения РФ № 572н, встать на учет в женскую консультацию должна каждая беременная до 12 недель и в каждом триместре пройти комплекс скрининг-исследований. Задача такой диагностики заключается в выявлении наиболее частых патологий развития плода, в частности синдромов Дауна, Эдвардса и Патау.
Стандартный пренатальный скрининг
В I и II триместрах беременности диагностика включает биохимический анализ крови на патологию плода по наличию уровней сывороточных маркеров:
- 11-14 недель − PAPP-А и бета-ХГ;
- 16-18 недель −ХГЧ, эстриол, α-фетопротеин.
Кровь нужно сдавать на голодный желудок. Уровень сывороточных маркеров (гормонов) у матери, носящей плод с возможными хромосомными аномалиями, будет отличаться от нормально развивающегося. К тому же при расчёте учитываются анамнез, регион проживания и другие многие показатели. Если на основании этих анализов женщина попадает в группу риска, ей будет предложена дополнительная диагностика.
В обязательный скрининг также входит ультразвуковая диагностика органов малого таза, которая проводится на сроках:
- 11-14 недель − для оценки строения органов плода и грубых пороках развития;
- 18-21 недели − для более точного определения анатомии внутренних органов и выявлении аномалий развития;
- 30-34 недели − для определения количества околоплодных вод, размеров и веса плода, его предлежания, исключения патологий, которые могут появиться на поздних сроках.
Врач, который будет проводить УЗИ, должен быть осведомлен о результатах биохимического скрининга крови.
Ультразвуковые маркеры хромосомных патологий плода включают ряд грубых пороков развития, которые уже в некоторых случаях можно обнаружить на первом обследовании. В первую очередь врач обращает внимание на толщину воротникового пространства (ТВП). Нормой считаются показатели: 11 недель − 1-2 мм, 13 недель, 6 дней − 2,8 мм.
Если показатели выше, то это не говорит сразу о генетической патологии, так как следует изучить остальные ультразвуковые признаки:
- гипоплазия (уменьшение) или аплазия (отсутствие) косточки носа;
- гиперэхогенность, то есть «яркость» кишечника на УЗ-изображении;
- повышенная «яркость» участка сердечной мышцы (желудочка сердца);
- одна артерия пуповины (норма − 2 артерии, 1 вена);
- кисты сосудистых сплетений в головном мозге плода.
Ультразвуковая диагностика информативна только до 80%. Выявленные подозрения на геномное заболевание у будущего ребенка, не считаются показанием для прерывания беременности, а говорят о необходимости дополнительных исследований.
Для более точной дородовой диагностики используют методы:
- неинвазивные − без взятия тканей плода по крови матери и УЗИ;
- инвазивные − с взятием тканей хориона, околоплодных вод или пуповинной крови.
Неинвазивная пренатальная диагностика
С 10 недели беременной с подозрением на патологию плода может быть назначен неинвазивный пренатальный тест ДНК (НИПТ). Это новый современный метод диагностики, который основывается на применении высокотехнологичных молекулярно-генетических методик, дающих возможность исследовать ДНК будущего ребенка. Материалом исследования становится кровь матери.

Тесты НИПТ включают целую линейку, направленную на выявление как одного синдрома Дауна, так и ряда микроделеционных нарушений, а также носительство генов наследственных заболеваний у матери. Информативность такого текста значительно выше стандартных анализов крови и, в зависимости от целей исследования, дает возможность выявить заболевание с точностью 99%.
Инвазивная пренатальная диагностика
На инвазивные методы исследования направляются беременные, у которых высокий суммарный (анализ крови, УЗИ, НИПТ) риск рождения ребенка с хромосомным заболеванием. Инвазивные процедуры назначаются по строгим показаниям и делаются только с письменного согласия женщины, так как существует небольшой риск осложнений (прерывания беременности не более 1%).
Вид исследования, который может назначить врач, зависит от срока беременности и материала анализа.
- На сроке 8-12 недель проводится биопсия ворсин хориона (клеток хориона, из которых состоит детская часть плаценты) с целью забор небольшого количества хориальной ткани.
- Наиболее оптимальным сроком для проведения амниоцентеза − с 15 по 20 неделю. Для анализа берут околоплодные воды, которые содержат клетки плода (пушковые волосы, чешуйки эпидермиса).
- Анализ пуповинной крови (кордоцентез) делается с 20-й недели беременности.
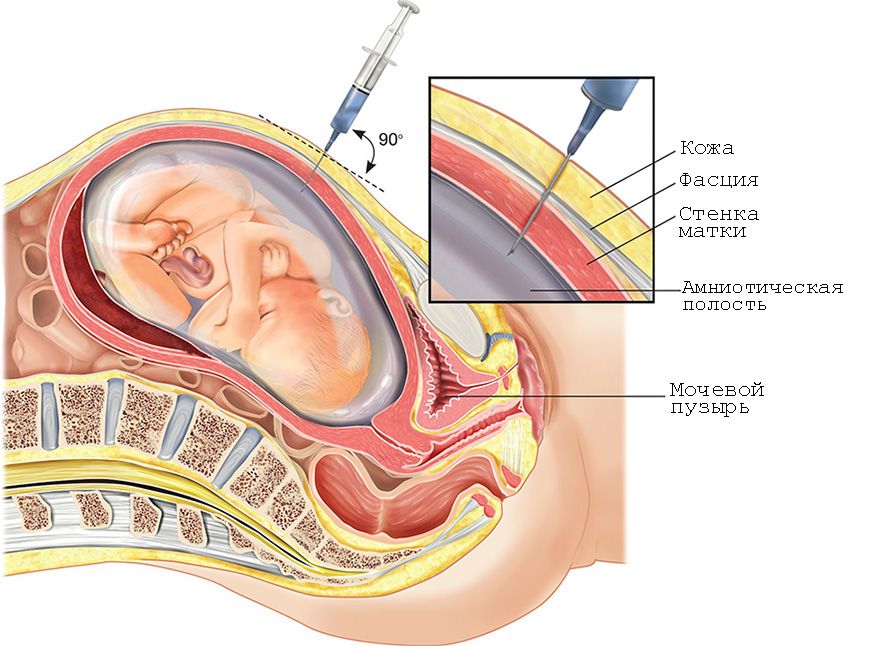
Процедуры проводятся под контролем УЗИ для уточнения срока беременности, контроля состояния тонуса матки и плода. Прокол осуществляется тонкой пункционной иглой через живот или шейку матки. Длится вся процедура не больше 15 минут и обычно не вызывает сильных болевых ощущений, поэтому обезболивание не применяется.
Инвазивные исследования противопоказаны при:
- остром воспалительном процессе с температурой и при обострении хронических заболеваний;
- повышенном тонусе матки и угрозе выкидыша;
- кровянистых выделений из половых путей;
- крупных новообразований матки.
Цель всех методов − цитогенетическое исследование взятого материала для определения кариотипа будущего ребенка и выявления возможных у него хромосомных аномалий. Кариотипирование осуществляется методом культивирования клеток с их дальней покраской и исследованием в световой микроскоп. Сроки получения результатов 3 недели и более.
Стандартный генетический анализ при беременности на кариотип методом рутиной покраски позволяет обнаружить только количественные и крупные структурные изменения хромосом. Слишком малые хромосомные нарушения, в частности микроделеции или микродупликации, не выявляются под световым микроскопом. В этом случае проводится так называемый «микроматричный хромосомный анализ».
Профилактика
К профилактическим мероприятиям хромосомных патологий в первую очередь относятся медико-генетические консультации, диспансеризация и пренатальная диагностика. Позиции профилактики основываются на оптимальном репродуктивном возрасте женщины (21-35 лет), отказ от деторождения в случае высокого риска патологий, а также отказ от деторождения в браках кровных родственников.

Чтобы исключить вероятность геномных заболеваний, важно осознанно подходить к родительству. На этапе планирования беременности будущим родителям, особенно из группы риска, не стоит пренебрегать медико-генетическим консультированием и при необходимости дополнительными обследованиями. Женщине обязательно нужно своевременно проходить плановые скрининг-исследования во всех триместрах беременности, что позволит оценить насколько велик риск патологий у плода. Существуют и ряд дополнительных методик пренатальной (дородовой) диагностики геномных мутаций у плода с точностью более 99%.
Мы сделали с мужем кариотипирование. Анализ показал, что у меня все в порядке, а у мужа − мужской кариотип со сбалансированной хромосомной перестройкой. У нас есть шанс родить здорового ребенка?
Анализы биохимии крови на гормоны после первого скрининга показали большую вероятность развития у ребенка синдрома Дауна, но на УЗИ никаких патологических изменений не видно. До этой беременности были 2 замершие на сроке 8 и 10 недель. Мой врач поднял вопрос о прерывании беременности, пока срок небольшой. Какие мне стоит сделать дополнительные исследования?
На УЗИ заподозрили синдром Эдвардса. Почему и что делать?

Действительно у синдрома Эдвардса (трисомия 18 хромосомы) есть особая симптоматика, которую можно увидеть у ребенка при проведении УЗД. Это малая величина плаценты, наличие одной пупочной артерии у плода, низкая частота сердечных сокращений и даже выраженные множественные аномалии развития. Но одной ультразвуковой диагностики для постановления такого диагноза недостаточно, так как косвенные признаки должны быть подтверждены генетическим исследованием. В зависимости от срока, лучше сделать биопсию ворсин хориона, анализ околоплодных вод или пуповинной крови с последующим кариотипированием клеток плода. Рекомендую проконсультироваться с генетиком, который разберется в вашей ситуации и назначит нужное исследование.
Мне 35 лет, было 3 замерших беременности на раннем сроке. После сделали с мужем тест на кариотип. Результат у меня − реципрокная транслокация между 15 и 16 хромосомой. Что нам делать в таком случае?

Вам лучше сделать ЭКО, но с преимплантационной генетической диагностикой эмбрионов. Отмечу, что отличить кариотип здорового эмбриона от носителя сбалансированной транслокации практически невозможно, поэтому у вашего ребенка может быть какая же хромосомная «ошибка». Но на его качество жизни, вероятно, это не повлияет. Также рекомендую в период беременности еще дополнительно провести пренатальный инвазивный скрининг плода.
Почему кровное родство родителей повышает риск редких наследственных заболеваний у ребенка?

В таких браках риск рождения детей с наследственными патологиями в 2 раза выше, так как оба родителя носители рецессивных мутаций в хромосомах и/или генах, которые у них не проявляются вследствие подавления доминантным аллелям. В результате родители визуально здоровы, а вероятность рождения ребенка с патологией составляет 25%. Для таких пар рекомендуется медико-генетическое консультирование с изучением здоровья, степени родства, возможных наследованных заболеваний в предыдущих поколениях, а также обязательное прохождение пренатальной генетической диагностики плода.
